BOJE, bojila (njem. Farbstoffe, tal. sostanze coloranti, engl. dyestuffs) su obojene prirodne i umjetne tvari, koje mogu bojiti različna druga tijela. Dijelimo ih prema podrijetlu i proizvodnji u anorganske i organske prirodne i umjetne boje. Među prirodne anorganske boje ubrajamo mineralne ili zemljane boje. Organske prirodne boje potječu iz biljnog ili životinjskog carstva. Umjetne su boje, izuzevši neke anorganske i metalne boje, ponajviše organske boje. Prema upotrebi dijelimo b. u tekstilne, slikarske, tiskarske i t. d. M. D-ć.
SADRŽAJ: Boja i kemijski sastav tvari, 5; Anorganske boje, 5; Organske boje, 6; Boje u kemijskom veleobrtu, 8; Boje za knjigotisak, 9; Postojanost boja, 9; Bojenje tekstilne robe, 9; Bojenje seljačko, 11; Bojenje stakla, 11; Bojenje tijela, 11.
Boja i kemijski sastav tvari. Kemijska teorija o organskim bojama govori o vezi, koja postoji između kemijskog sastava ili konstitucije tvari i njezine boje. Glavna je svrha te teorije, da posluži proizvodnji umjetnih organskih boja. Sve dotle, dok se nije znalo, kako su poredani pojedini atomi i atomske skupine u molekuli obojenih ugljikovih spojeva, bila je proizvodnja bojila prepuštana empiriji i slučaju. I doista su prve organske boje otkrivene pukim slučajem. Danas je kemizam, napose organskih boja, dobro poznat, pa je to upravo omogućilo golem razvitak umjetnih (katranskih ili anilinskih) boja.
Zasićeni alifatski spojevi apsorbiraju u skrajnjem ultraljubičastom dijelu spektra (ispod 200 mμ), pa su u bijelom svijetlu bezbojni. Aromatski ugljikovodik benzol, C
6H
6 apsorbira svijetlo dužine vala oko 270 mμ, pa je i on bezbojna bistra tekućina. Ako u molekulama spomenutih ugljikovodika dolaze neke nezasićene atomske skupine, pomiču one pruge apsorpcije iz ultraljubičastog dijela prema vidljivom dijelu spektra, pa spojevi postaju i za oko obojeni (→
boja). Alifatski ugljikovodici poprimaju boju, čim imaju najmanje 4 dvostruke C = C— veze u kontinuiranom položaju. U ovakvu skupinu spojeva ubrajamo mnoge važne prirodne boje zvane »karotinoidi«, na pr. žutu boju mrkve
(Daucus Carota), žutu boju žutanjka jajeta, boju žutog jesenjeg lišća, zatim crvenu boju paprike, rajčice, šipka i t. d. Najveći dio organskih boja ubrajamo u t. zv. aromatske spojeve, jer imaju u svom sastavu benzolove prstene ili kondenzirane sustave, koji su nastali iz benzolovih jezgara (na pr. naftalin, antracen i dr.). Aromatski je ugljikovodik bifenil, C
6H
5—C
6H
5 bezbojan (apsorbira kod neko 315 mμ), ako između fenila dolazi nezasićena etilenska skupina, —CH = CH—, nastaje spoj C
6H
5—CH = CH—C
6H
5, koji je još uvijek za oko bezbojan (apsorbira kod neko 345 mμ); ali ako između dvaju fenila dolaze četiri etilenske skupine, spoj je žute boje, jer se apsorpcija pomiče u vidljivi dio spektra, u područje između 400—800 mμ. S povećanjem broja nezasićenih skupina boja prelazi u narančastu, crveno narančastu i t. d.
Selektivna je apsorpcija svjetlosti u vezi s nezasićenošcu molekula. Prema tome je i boja ugljikovih spojeva zavisna o djelomično slabije vezanim elektronima u nezasićenim spojevima. Već su Graebe i Liebermann (1868) primijetili, da obojeni spojevi gube svoju boju, kada reduciranjem prelaze u zasićene spojeve. Apsorpcija je u vidljivom dijelu spektra uvjetovana nekim određenim i posebnim nezasićenim atomskim skupinama u molekuli. Takve je skupine nazvao O. N Witt (1876) kromofornim skupinama. Kromofori (nosioci boje) uzrokuju pomak apsorpcije u vidljiv dio spektra. Najvažniji su kromofori, osim spomenute etilenske skupine, (—CH = CH—), karbonil ( = C = O), nitrozo (—N = O), nitro (—NO2), azo (—N = N—) i dr. Vrlo kromoforno djeluju nitrozo-skupine i azo-skupine, potonja samo u aromatskom sustavu (azometan je bezbojan). Jedna kromoforna skupina redovno još nije dovoljna, da spoj bude obojen. Ima međutim spojeva, kojih je selektivna apsorpcija svjetlosti zavisna o nepostojanom ili nezasićenom stanju pojedinog atoma ili atomskog veza. I ako takvi spojevi nemaju dvostrukih veza u molekuli, ipak su obojeni (na pr. jodoform, CHJ3).
Organske spojeve s kromofornim skupinama zovemo kromogenima (stvaraoci boje). Kromogeni redovno još nisu bojila (na pr. nitrobenzol ili narančasto obojeni azobenzol). Zato je potrebna još jedna skupina, koja svojom kemijskom prirodom veže obojene tvari s tekstilnim vlakancima. Usput spominjemo, da je najvažnija upotreba organskih boja u bojenju tkanina i tekstilnih proizvoda. Skupine, koje mogu pojačati djelovanje kromofora, zovemo auksokromnim skupinama. U sintetskoj kemiji organskih boja služe kao auksokromi: fenolske hidroksilne (oksi) skupine, aromatski vezane amino-skupine i njihovi derivati; uopće skupine, koje mogu stvarati soli (OH, NH2, SO3H, COOH). Prema tome imamo kisela i bazična bojila. Same auksokromne skupine nemaju kromoforna svojstva, ali mogu znatno utjecati na boju kromogena tako, da je razviju ili pojačaju. Od kromogena postaje organsko tehničko bojilo istom onda, ako se kemijskom sintezom u molekulu uvede jedna ili više auksokromnih skupina.
Vuna i svila su bjelančevinama slične tvari, a poznato je, da su bjelančevine amfoterne prirode i da mogu stvarati spojeve i s kiselinama i bazama. Upravo zato možemo vunu i pravu svilu bojiti neposredno bojilima, koja imaju auksokromne skupine u molekuli. Pamuk je gotovo kemijski čista celuloza, zato se redovno ne spaja neposredno s kiselim i bazičnim bojama. Zbog toga se pamuk prije bojenja stavlja u močila (Beizmittel), a to su otopine različnih kemijskih tvari, koje se u koloidnoj adsorpciji vežu uz vlakanca pamuka. Nakon toga se može bojilo kemijski čvrsto vezati uz vlakna, i to u obliku kompleksnih spojeva. Kao močila služe za kisele boje najčešće hidroksidi kroma, aluminija, željeza, antimona i kositera, dok za bazične boje služi najčešće tanin.
LIT.: H. Kauffmann Über den Zusammenhang zwischen Farbe und Konstitution bei chemischen Verbindungen, Stuttgart 1904; Isti, Die Auxochrome, Stuttgart 1907; Witzingcr, Organische Farbstoffe, 1933; Martinet, Couleur et Constitution chimique, Pariz 1924; G. Panizzon, Trattato di chimica delle sostanze coloranti, Milan 1918; J. K. Wood, Chemistry of Dyeing, London 1926; F. Ullmann, Enziklopädie der Technischen Chemie, Berlin i Beč 1930. M. D-ć.
Anorganske boje služe u slikarstvu i tehnici, a imaju karakter pigmenata, t. j. sitnih, u vodi ili ulju netopljivih obojenih čestica, koje se s pomoću kojeg sredstva za fiksiranje vežu za podlogu. Kao sredstvo za fiksiranje pigmenta može služiti laneno ulje (uljene boje), emulzija ulja i vode uz dodatak raznih bjelančevina kao emulzifikatora (tempera boje) ili biljno ili životinjsko ljepilo (vodene boje). Već u prethistorijsko doba služio se čovjek raznim prirodnim bojama: žutim i crvenim okerom, zelenom zemljom (terre verte), azuritom i malahitom, rumenicom i auripigmentom, čađom i kredom. Uz ove prirodne boje počela je u starom vijeku proizvodnja umjetnih anorganskih boja: egipatskog modrila (kalcijev-bakreni silikat), olovne gleđe i minija (olovni oksidi), te olovnog bjelila (bazični olovni karbonat). U srednjem je vijeku, najprije u Bizantu, ultramarin (smrvljen i vodom plavljen lazurit, prirodni natrijev aluminijev silikat s nešto natrijeva sulfida) zamijenio egipatsko modrilo, jer se vještina pripravljanja te boje izgubila u metežu, kad je propalo rimsko carstvo. Na početku novog vijeka nadošla je još smalta (smrvljeno kobaltovo staklo ljubičaste boje), umjetno priređeni karbonati bakra i napuljsko žutilo (olovni antimonat). U 18. i 19. st. otkriven je velik broj novih umjetnih anorganskih boja.
Danas se kod upotrebe anorganskih boja pazi na to, da boje dobro pokrivaju, t. j. da su već u tankom sloju potpuno neprozirne, da su postojane na zraku i svijetlu, a kod njihove tehničke upotrebe traži se još, da nisu otrovne. Iz posljednjeg razloga zabranjena je danas tehnička upotreba olovnog bjelila i švajnfurtskog zelenila (bakreni acetat-arsenit), premda boje odgovaraju drugim zahtjevima, pa i danas služe u slikarstvu u ograničenoj mjeri.
Od anorganskih su boja najvažnije:
Bijele boje: Olovno bjelilo, pokriva vrlo dobro, ali nije posve postojano, jer s vremenom crni. Cinkovo bjelilo (cinkov oksid), pokriva slabije, ali je postojanije od olovnog bjelila i pritom neotrovno. Titanovo bjelilo (titanov oksid), pokriva vrlo dobro, ali neke vrste na svijetlu posive. Litopon (smjesa cinkova sulfida i barijeva sulfata), jeftina je boja, koja služi za pokrivanje podloge. Kreda (kalcijev karbonat), služi u prvom redu kao jeftina vodena boja u tehnici za pokrivanje velikih površina.
Žute boje: Napolitansko žutilo, dobro pokriva i vrlo je postojano. Veliki broj žutih boja daje kromna kiselina, koje se soli s nekim kovinama (olovo, cink, barij, stroncij) danas mnogo upotrebljavaju kao boje. Namiješane s uljem nisu na svijetlu sasvim postojane, a olovni kromat (kromovo žutilo), koji se najviše upotrebljava, usto je i otrovan. Kadmijevo žutilo (kadmijev sulfid) pokriva dobro i nije otrovno, ali se radi visoke cijene upotrebljava samo u slikarstvu. Oker (prirodni aluminijev hidrosilikat, koji sadržava nešto željeza), ako je čist, vrlo je postojan, a usto jeftin, pa mnogo služi u tehnici. Neke vrsti poznate su pod imenom terra di Siena.
Crvene boje: Crveni oker, dolazi u prirodi kao terra rossa i terra di Treviso, a pravi se i umjetno žarenjem žutoga okera. Željezni oksid (Fe2O3) služi u tehnici kao jeftina i postojana crvena boja. Rumenica, cinober (živin sulfid), neke vrste nisu na svijetlu sasvim postojane, jer s vremenom potamne. Boja nije otrovna, jer je u vodi i kiselinama posve netopljiva. Minij (olovni oksid Pb3O4) se upotrebljavao u srednjem vijeku mnogo kao zamjena za skupu rumenicu kod ukrašivanja rukopisa (otud ime minijature). Danas služi za premazivanje željeznih konstrukcija, da bi se zaštitile od rđe.
Modre boje: Ultramarin, dobiva se danas umjetno žarenjem bijele gline s natrijevim sulfatom i ugljenom. Boja je postojana na svijetlu i jeftina. Kobaltovo modrilo (žaren aluminijev oksid uz dodatak male količine kobaltova oksida) postojana je i neotrovna boja. Berlinsko (parisko) modrilo (feri-ferocijanid, Fe4[Fe C6N6]3), pokriva vrlo dobro, na zraku i svijetlu je postojano i pritom neotrovno, pa se mnogo upotrebljava.
Zelene boje: Švajnfurtsko zelenilo, dobro pokriva i postojano je, ali je veoma otrovno, stoga mu je upotreba u tehnici zabranjena, a i u slikarstvu se izbjegava. Kromovo zelenilo (kromov oksid, koji sadržava nešto vode, Cr2O3 + H2O), postojana je i neotrovna boja. Kobaltovo (Rinmannovo) zelenilo (žaren cinkov oksid uz dodatak male količine kobaltova oksida), slabo pokriva, ali je veoma postojano.
Smeđe boje: Umbra (prirodni aluminijev hidrosilikat, koji sadržava nešto mangana i željeza), s vremenom tamni.
Crne boje: Kao crna boja najviše se upotrebljava ugljik u raznim oblicima (čađa, drveni i koštani ugljen, rjeđe grafit). Pokriva vrlo dobro i vrlo je postojan. Osim toga upotrebljava se još željezni oksid (Fe2O3) i manganovo crnilo (manganov dioksid, MnO2), koji su također postojani, ali slabije pokrivaju.
LIT.: A. Eibner, Malmaterialienkunde als Grundlage der Maltechnik, Berlin 1909; M. Doerner, Malmaterial und seine Verwendung im Bilde, 6 izd., Stuttgart 1938; F. Rose, Die Mineralfarben, Leipzig 1916; Ch. Cottignies, Couleurs et peintures, Pariz 1924; F. W. Weber, Artists’ Pigments, New York. S. M.
Organske boje. Gotovo su sve prirodne i umjetne organske boje ciklični spojevi; derivati benzola, naftalina, antracena, karbazola i t. d. Danas se skoro sve organske boje dobivaju iz katrana kamenog ugljena, zato se i zovu katranske ili anilinske boje. U trgovini ima oko desetak tisuća tih boja.
Prvi temelj i poticaj za proizvodnju umjetnih katranskih boja dala su otkrića mauveina, ljubičaste boje, po Perkinu (1856), i fuksina, crvene boje, po Verguinu (1859). Organske se boje upotrebljavaju za bojenje i tiskanje tekstilnih vlakanaca, pređe i tkanina iz vune, pamuka, svile, umjetne svile, celulozne vune, lana, jute i t. d., nadalje za bojenje kože, papira, slame, drva, umjetnog cvijeća, perja, masti, voska, sapuna, tinte, živežnih namirnica, pokosti, lakova i t. d. U analitičkoj kemiji služe mnoge organske boje kao indikatori (Methylorange, Phenolphthalein i t. d.). U histologiji i bakteriologiji služe za bojenje mikroskopskih preparata, a u fotografiji za senzibiliziranje fotografskih emulzija. Organske se boje dijele kemijski: u nitroso-, nitro-, azo-, diazo-, tiazol-, difenilmetanske, trifenilmetanske, rosanilinske, antrakinonske, oksiketonske, kinolinske, indigo, indigoidne boje i t. d. Zajednička kemijska karakteristika svih organskih boja jest njihova nezasićenost. Obojenost međutim ne zavisi samo o broju i razmještaju dvostrukih vezova i nezasićenosti jednog ili više atoma, nego i o općoj molekularnoj konstituciji.
Danas dijelimo organske boje po metodama rada u glavnom području njihove upotrebe, t. j. u tekstilnoj proizvodnji, bez obzira na njihovu konstituciju na one, koje su: A. u vodi topive: 1. kisele boje, 2. bazične boje, 3. substantivne ili direktne boje, 4. boje na močila (Beizenfarbstoffe); B. u vodi netopive: 1. sumporne boje, 2. moćne boje (Küpenfarbstoffe), 3. boje na močila (netopive u vodi), 4. boje, koje se grade na vlaknu (Entwicklungsfarbstoffe), 5. boje za acetatnu svilu, 6. boje topive u organskim topilima.
U trgovinu dolaze organske boje pod različnim nazivima, koji su djelomično odabrani samovoljno, a djelomično vezani na njihovu užu kemijsku konstituciju ili na način upotrebe, kao na pr. Chrysoidin-, Auramin-, Methylen-, Phosphin-, Diamin-, Benzidin-, Chlorantin-, Chloramin-, Diazo-, Sirius-, Eliamin-, Benzochrom-, Immedial-, Sulfogen-, Pyrogen-, Anthralan-, Alizarin-, Palatinecht-, Neolan-, Indanthren-, Cibanon-, Sandothren-, Romanthren-, Helindon-, Antinol-, Tinonchlor-, Indigosol-, Naphtol AS-, Ultrazol-, Cibanaphtol-, Irganaphtol-, Rapidogen-, Rapidecht-, Neocoton-boje i t. d.
Spomenuta otkrića prve sintetske organske boje mauveina po Perkinu (1856) i fuksina po Verguinu (1859), nadalje veoma značajni radovi Gräbea, Liebermanna, Caroa i Perkina oko određivanja konstitucije i sinteze alizarina te radova A. v. Baeyera na sintezi indiga dali su poticaj čitavim plejadama kemičara za najsmjelije kemijske sinteze organskih boja.
Spoznaja, da katran kamenog ugljena sadrži mnoge aromatske spojeve (benzol, toluol, ksilol, fenol, krezole, naftalin i antracen), koji služe kao kemijsko gradivo za sve organske boje, učinila je katran glavnom sirovinom organske kemijske proizvodnje. Za proizvodnju organskih boja katran se najprije odijeli sedimentacijom od amonijačne vode, a zatim se podvrgne frakcioniranoj destilaciji. Prva frakcija (do 170º C) je t. zv. lako ulje; sadrži u glavnom benzol i njegove homologe. Druga frakcija (do 270ºC) je teško ulje; sadrži naftalin, fenole sa visokim vrelištem, kinolinske baze i t. d. Treća frakcija (do 400º C) sadrži velike količine antracena, pa se zove antracensko ili, po zelenoj boji, zeleno ulje; destilira se najčešće u vakuumu. Dalji destilat nema značaja za veleobrt organskih boja. Ostatak je paklina ili smola, koja se upotrebljava za izradbu briketa, gradnju cesta, krovnu ljepenku i t. d. Pojedine se frakcije dalje destilacijom dijele, čiste i upotrebljavaju kao ishodni proizvodi za kemijsku sintezu. Od benzola i njegovih derivata dobivamo nitriranjem t. zv. nitro-spojeve, a iz ovih redukcijom amino-spojeve: naime anilin (C6H5NH2), orto- i para-toluidin i ksilidine, koji su važni međuproizvodi za sintezu organskih boja, radi toga zvane i anilinske ili katranske boje. Sulfuriranjem benzola i njegovih derivata dolazimo do sulfokiselina, a taljenjem ovih sa natrijskom lužinom do još važnijih hidroksilnih derivata i do veoma važne salicilne kiseline. I kloriranjem postizava kemijska sinteza važne poluproizvode za pripremu organskih boja. Naftalin daje nitriranjem, sulfuriranjem i taljenjem s alkalijama veoma važne naftole, naftilamine i njihove sulfokiseline. Tako na pr. nitriranjem naftalina nastaje α-nitronaftalin (uz nešto β-spoja) i dalje redukcijom α-naftilamin, također važna komponenta organskih boja. Sulfuriranjem naftalina dobivamo α- i β-naftalinmonosulfo kiseline, a iz ovih izvanredno važne α- i β-naftol.
Veoma veliku važnost postigli su u novije doba derivati antracena, napose antrakinon i alizarin. Iz ovih intermedijarnih proizvoda nastaje diazotiranjem (t. j. uvođenjem karakteristične azo-skupine —N = N— s pomoću dušičaste kiseline) i vezanjem diazo-spojeva s drugom komponentom iz benzolskog i naftalinskog reda veliki broj azo-boja (oksiazo-, diazo-, poliazo-). Azo-boje su veoma važne. Boje jednostavnih molekula su žute i narančaste, dok uvođenjem različnih skupina u molekulu prelaze u crvenu, modru, smeđu i crnu boju. Navest ćemo kao primjer nekoliko tipova azo-boja:
Anilin + m-fenilendiamin:
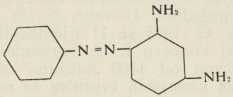 CHRYSOIDIN (Caro 1875, Witt 1876)
CHRYSOIDIN (Caro 1875, Witt 1876)Anilin + amidonaftolsulfokiselina 1. 8. 4. 6:
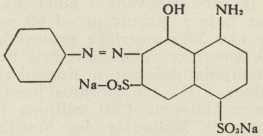 TOLAN-CRVENILO B (Rosenberg i Krecke 1893)
TOLAN-CRVENILO B (Rosenberg i Krecke 1893)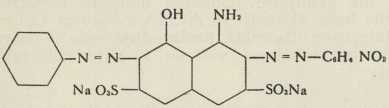 NAPHTOL CRNILO (Hoffmann 1891)
NAPHTOL CRNILO (Hoffmann 1891)S tehnološkog gledišta značajne su trifenilmetanske boje, od kojih je najvažniji fuksin:
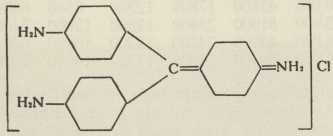 FUKSIN ili ROSANILIN (Veguin 1859)
FUKSIN ili ROSANILIN (Veguin 1859)Za određenje konstitucije trifenilmetanskih boja zaslužni su osobito E. i O. Fischer.
U novije vrijeme osobito se razvila djelatnost kemičara učenjaka i tehničara na području derivata antracena, t. zv. antrakinonskih boja. Najstarije su organske boje ove skupine oksi-antrakinonske boje i njihovi derivati, alizarin (1, 2-dioksiantrakinon):
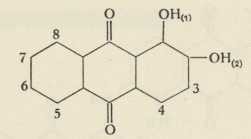 ALIZARIN (Gräbe i Liebermann)
ALIZARIN (Gräbe i Liebermann)nitroalizarin, alizarin-plava, neki trioksiantrakinoni i t. d. Ovi spojevi sadrže kao i alizarin dvije hidroksilne skupine u orto-položaju (1, 2), pa ih zato i nazivaju alizarinskim bojama. Boja oksiantrakinona ovisi uglavnom o položaju hidroksilnih skupina: α-položaj uvjetuje crvenu do plave boje, β-položaj žutu do smeđe boje. Vanredno velika postojanost ovih boja, u obojenju na tekstilnim vlaknima, dala je poticaj veleobrtu boja, da izgradi daljne derivate alizarina. Nitriranjem nastaje β-mononitroalizarin:
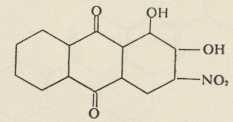 ALIZARINORANGE (Strobel)
ALIZARINORANGE (Strobel)Zagrijavanjem s glicerinom i sumpornom kiselinom nastaje iz gornjeg spoja dioksiantrakinon-kinolin:
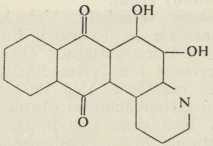 ALIZARIN-MODRA (otkrio Prudhomme 1877, konstitucija Gräbe)
ALIZARIN-MODRA (otkrio Prudhomme 1877, konstitucija Gräbe)Genijalno otkriće R. Bohna (1888), da djelovanjem dimeće se sumporne kiseline (oleuma) nastaju polioksiproizvodi prema shemi:
koje je Schmidt proširio na antrakinon, alizarin i sve antrakinonske derivate i upotpunio na tetra-, penta- i heksa-oksiantrakinonske spojeve, otvorilo je put proizvodnji velikoga broja novih prekrasnih postojanih boja.
Sinteza indiga i to iz izo-nitrocimetne kiseline (Baeyer) i fenilglicinortokarbonske kiseline (Heumann):
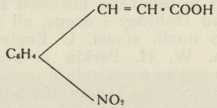 (Baeyer 1880)
(Baeyer 1880)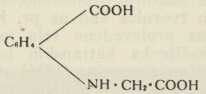 (Heumann)
(Heumann)te iz fenilglikokola: C6H5. NH. CH2. COOH (Heumann):
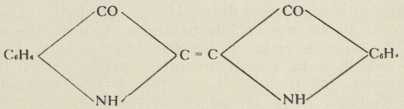 INDIGO
INDIGOpa konačno otkriće indantrena (Bohn 1901):
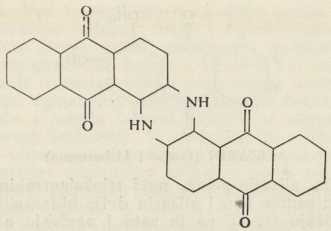 INDANTREN MODRA
INDANTREN MODRA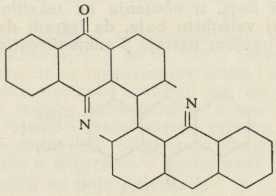 INDANTREN ŽUTA
INDANTREN ŽUTAdo sada najstalnijih tekstilnih boja, otvorili su nove mogućnosti na području sinteze organskih boja, kojih je industrija danas na velikoj visini. M. V-ć.
Boje u kemijskom veleobrtu. Veleobrtna proizvodnja katranskih boja nastala je doduše u Engleskoj i Francuskoj, ali se nakon otkrića umjetnog alizarina (Liebermann i Graebe 1868) prenosi i u Njemačku, gdje se vrlo brzo razvija do velikih razmjera. Već 1860 osnovana je prva tvornica fuksina u Offenbachu na Majni i druga Fr. Bayer u Elberfeldu. G. 1863 osnovana je tt. Meister Lucius i Brüning u Höchstu na Majni. Badische Anilin und Sodafabrik, Ludwigshafen a. Rh. nastala je 1865, Agfa 1867 i E. Cassella 1870. Osobit zamah zauzima proizvodnja nakon 1877, kad je stupio na snagu novi njemački patentni zakon. Po tom zakonu nije zaštićen novi produkt kao takav, kao što je to bilo u Francuskoj, nego samo postupak za njegovo dobivanje. Sve do 1913 ostaje Njemačka glavnim proizvođačem i središtem veleobrtne proizvodnje boja, a tek iza nje dolazi Švicarska, koje je udio kod razvitka proizvodnje boja veoma znatan. Već odavna su švicarski kemičari usavršavali i pojeftinjavali mnoge postupke za dobivanje boja, koji su bili izrađeni u drugim zemljama, a pronašli su i štošta novog, kao na pr. dobivanje safranina i drugih boja. U Francuskoj bilo je osim podružnica njemačkih i švicarskih poduzeća samo jedno znatnije poduzeće, Société Anonyme des Matières Colorantes et Produits Chimiques de St. Denis de Paris. No ovo poduzeće je po svom opsegu bilo manje od mnogih malih njemačkih tvornica. Francuska je ipak na području pronalazaka pridonijela mnogo daljnjemu razvitku: tako je na primjer prvi praktički iskoristivi postupak za dobivanje anilina redukcijom nitrobenzola sa željezom izradio Francuz Béchamp. U Engleskoj nije od 1887 (otkriće primulina) dugo vremena ništa znatnije pronađeno. Bilo je osnovano nekoliko znatnijih tvornica kao na pr. Read Holliday i druge, ali je u ovima proizvedeno vrlo malo novih stvari. U Engleskoj je kolijevka katranskih boja. W. H. Perkin je svojim otkrićem mauveina (1856) utro put za proizvodnju umjetnih boja te je 1857 podigao prvu tvornicu katranskih boja u Grenford Greenu kraj Londona.
Od 1877 do 1913 napreduje razvitak proizvodnje boja u Njemačkoj orijaškim koracima, dok u ostalim zemljama, osim u Švicarskoj, ova proizvodnja sve više nazaduje, tako da se 1913 može govoriti upravo o njemačkoj hegemoniji na području proizvodnje boja. U tom razdoblju prijavljeno je oko 10.000 njemačkih patenata, koji zaštićuju najmanje 50 hiljada boja. Od toga dolazi u trgovinu oko 1000 posebnih boja, što odgovara od prilike 10.000 trgovačkih maraka. Od ovih 1000 posebnih boja otkrili su francuski i engleski kemičari po 30, švicarski 150, a njemački 700 boja. Golem napredak njemačke veleobrtne proizvodnje boja do 1913 vidi se iz ove tablice (brojke su u milijunima maraka):
|
Godina
|
Njemačka
|
Engleska
|
Francuska
|
Švicarska
|
USA
|
|
1878
|
45
|
9
|
5
|
3
|
—
|
|
1895
|
100
|
—
|
—
|
12
|
—
|
|
1905
|
180
|
—
|
—
|
16
|
—
|
|
1913
|
280
|
5
|
3.5
|
20
|
8
|
Ovdje je nabrojena samo vlastita proizvodnja pojedinih zemalja. U istinu su francuske, engleske i američke podružnice njemačkih tvornica proizvodile znatne količine boja iz nuzproizvoda uvezenih iz Njemačke. Ukupna potrošnja katranskih boja cijenila se 1913 na 150.000 tona u vrijednosti od 385 milijuna maraka.
Poslije svjetskog rata položaj se promijenio u toliko, što su Francuska, Engleska i Amerika počele samostalno proizvoditi boje i to u daleko većoj mjeri, nego je odgovaralo vlastitoj potrošnji. Uslijed toga su te zemlje počele u znatnoj mjeri izvoziti pojedine boje, tako da je naročito u Istočnoj Aziji došlo do živahne konkurentske borbe. Naravno da je radi toga i njemačka proizvodnja i izvozna trgovina donekle nazadovala. No njemačka se nauka i veleobrtna proizvodnja s pomoću svoje visoke tradicije ponovno podigla, proširivši svoje djelovanje na nova područja, osobito polažući važnost na skuplje stalne boje, kao na pr. boje u močama (Indanthreni), Naphtol-AS boje, te osobito stalne no i mnogo skuplje boje drugih skupina.
Kasnije je uslijed međunarodnih odnošaja došlo do sporazuma između pojedinih tvornica te do stvaranja novih velikih grupacija G. 1925 se 11 njemačkih tvornica boja ujedinilo u veliki koncern I. G. Farbenindustrie A. G. s početnom glavnicom od 1100 milijuna maraka. K tomu je pridošlo još 28 kemijskih tvornica sa srodnih područja tako, da ta skupina tvori danas jednu od najvećih zajednica kemijskog veleobrta I u međunarodnom mjerilu došlo je do sporazuma i to 1929 između njemačkih, švicarskih i francuskih poduzeća, a 1932 između engleskih i njemačkih poduzeća. U Americi je također došlo do koncentracije, pa je 1929 osnovana i američka interesna zajednica tvornica boja s glavnicom od 60 milijuna dolara, koja kontrolira oko 30% američke proizvodnje boja. Glavni predstavnik američke veleproizvodnje boja je koncern Dupont (250 milijuna dolara); u Engleskoj su kemijske tvornice okupljene u ICI (56 milijuna funti), a u Francuskoj u Kuhlmann koncernu (300 milijuna franaka) u zajednici s Compagnie Nationale des Matières Colorantes de St. Denis (40 milijuna franaka). Švicarska poduzeća: Gesellschaft für chemische Industrie in Basel (Ciba), Chemische Fabrik vorm. Sandoz, Basel, J. R. Geigy, Durande Huguenin, također su se zbila i posjeduju u Engleskoj i Americi zajedničke podružnice. Osim u ovim zemljama još je od važnosti proizvodnja boja u Italiji, gdje također postoji niz kemijskih poduzeća odnosno koncerna, koji proizvode boje. Glavniji su ACNA i Fabrica Colori d’anilina, Malegnano. Razvitak proizvodnje boja u najvažnijim industrijskim zemljama vidi se iz slijedećih tablica (u tonama):
|
Godina
|
Njemačka
|
U. S. A.
|
Engleska
|
Francuska
|
Švicarska
|
Italija
|
Japan
|
|
1913
|
125.000
|
3300
|
2000
|
1550
|
8000
|
—
|
—
|
|
1920
|
47.000
|
28000
|
23000
|
7350
|
10500
|
—
|
—
|
|
1922
|
92.700
|
29000
|
9300
|
8060
|
5000
|
—
|
—
|
|
1927
|
80.000
|
42700
|
17800
|
12500
|
8500
|
6000
|
7800
|
|
1929
|
75.000
|
51000
|
25400
|
12800
|
12000
|
7400
|
8000
|
|
1933
|
66.000
|
45900
|
24100
|
12200
|
10000
|
6200
|
16000
|
|
1934
|
76.000
|
39000
|
24000
|
11300
|
10000
|
7000
|
18400
|
Čitav razvitak proizvodnje boja, počevši od prvih mršavih početaka umjetnog dobivanja boja u Engleskoj pa sve do danas, zahvaljuje svoj veliki uspon uglavnom njemačkim kemičarima. U tom razvitku mogu se jasno razabrati tri odsjeka. U prvom odsjeku traže se nove boje, posve empirijski, ali s mnogo uspjeha. Na osnovi iskustva izgrađeno je i upoznavanje strukture novih spojeva, kao rezultat Kékuléove teorije benzolove jezgre. Upoznavanjem strukture mogle su biti izgrađene i nove sinteze, kojima današnja veleobrtna proizvodnja boja zahvaljuje svoje velike uspjehe. No i u ovom drugom odsjeku bio je glavni cilj otkrivanje novih boja bez osobitih obzira na bojadisarska svojstva. Tek u posljednjem trećem odsjeku dolazi do međusobnog upliva proizvodnje i potrošnje tako, da se ne teži samo za povećanom postojanosti, nego i za tim, da se boje mogu što jednostavnije primjenjivati.
Po kemijskom sastavu otpada od ukupne proizvodnje 50% na azo-boje, 14% na sumporno crnilo, 9.4% na trifenilmetanske i druge boje, 8.8% na antracenske i boje u močama, 7% na indigo, 4.7% na ostale sumporne boje.
Proizvodnja boja iznosi zapravo samo manji dio ukupne proizvodnje u velikim kemijskim poduzećima, a i narodno-gospodarsko značenje ove grane veleobrta nije baš osobito znatno. S druge strane povisuje bojadisanje u velikoj mjeri vrijednost tekstilne robe. Prema procjeni »Odbora za istraživanje uvjeta proizvodnje i prodaje njemačke privrede« iznosi ukupna vrijednost svjetske proizvodnje boja oko 700 milijuna maraka; vrijednost nebojadisanih tekstilija u svijetu cijeni se na 21 milijardu maraka, a bojadisanih na 20—35 milijardi maraka, što iznosi 10—14% od ukupne svjetske veleobrtne proizvodnje, koja se je cijenila 1928/29 na 225 milijarda maraka. M. Ž.
Boje za knjigotisak, koje se upotrebljavaju kod tiska, izrađuju se u posebnim tvornicama (kod nas: tvornica boja i pokosti »Chromos« d. d., Zagreb-Samobor). Tiskarske se boje sastoje od fino razdijeljene boje u svijetloj pokosti. Kod tiska prodire u papir samo neznatan dio pokosti; najveći dio ostaje pomiješan s bojom na površini papira i tamo oksidira kod sušenja, pri čemu se tiskarska boja čvrsto veže s papirom pod djelovanjem pokosti, koja je prodrla u papir. Tiskarske se boje dijele u dvije glavne skupine: u šarene i nešarene. U nešarene spadaju bijela i crna boja (tiskarsko crnilo), kao i svi među njima sivi tonovi. Fino tiskarsko crnilo se sastoji od fine lanene pokosti i najbolje čađe. Crna boja za knjige i novine izrađuje se naprotiv od teških ulja, parafinskog ulja, kolofonija i jeftine čađe. Kod šarenih boja mogu se upotrijebiti samo neke zemljane boje, kovinske boje i takve organske boje, koje su za to podesne. Danas se najviše upotrebljavaju katranske boje, koje su netopive u vodi, pa se vežu s pomoću punila (kaolin, aluminijski hidroksid i t. d.). S. H.
Uglavnom postoje tri vrsti boje za štampu u knjigotisku, litografiji i ofsetu, odnosno bakrotisku. Međusobno se ove boje razlikuju svojom jakošću, gustoćom. Boja se odabire prema kakvoći papira, predmetu koji se ima štampati ili kod štampanja autotipija prema gustoći mreže i dubini jetkanja. Postoji pet temeljnih boja: crna, žuta, crvena, modra, bijela. Spajanjem ovih boja dobivaju se najrazličitije vrste i nijanse. U boju većinom tamnijeg tona primiješa se još jedna anilinska boja, koja se s prvom samo slabo spaja, čime se postizavaju tonski efekti. J. K.
Postojanost boja. Organske i anorganske boje kemijski su spojevi, koji dolaze u promet u obliku kristalića u prahu ili u tijestu kao fina kemijska roba. One služe za bojadisanje tekstilnih vlakanaca, papira, kože, slame, drva, gume, anorganskih pigmenata, ulja, masti, voskova i t. d.
Dok su kod veoma ograničenoga broja anorganskih boja, koje se još danas upotrebljavaju, postojanosti na temelju starih iskustava opće poznate, kod organskih, sintetički dobivenih boja, kojima broj danomice raste, nastoji primijenjena kemija provesti točnu klasifikaciju prema postojanostima. Postojanosti njihovih obojenja izražavaju se u brojkama, koje označuju stupanj postojanosti, a koje su određene prema propisima stanovitih kemijskih, odnosno kemijsko-tekstilnih društava ili prema praktičkim iskustvima proizvađačkih tvornica. Tako na pr. za njemačku proizvodnju boja vrijede propisi i tipovi komisije za postojanosti u društvu njemačkih kemičara (Echtheitskom-mission im Verein deutscher Chemiker), prema kojima za postojanost obojenja prema svijetlu postoji skala od 8, a za sve druge postojanosti skala od 5 brojeva.
Kako postojanosti ovise u različnim omjerima i o jačini obojenja, to se kod postojanosti obojenja prema svijetlu, koje je najvažnije, u najnovije vrijeme ova skala proširila tako, da se postojanost označuje uz određenu jačinu obojenja (Richttyp) i za 2 slabija obojenja (⅓, ⅙, Richttyp).
U tu svrhu izrađena je za sve vrsti tekstilnih vlakanaca (do sada uglavnom za pamuk i vunu) posebna skala pomoćnih tipova obojenja, prema kojoj se određuje normalni tip jačine.
Tekstilni veleobrt kao glavni potrošač boja dobivenih iz katrana kamenog ugljena razlikuje uglavnom postojanosti, koje su potrebne u proizvodnji, od onih, koje su potrebne kod potrošnje tekstilne robe.
Kao glavne postojanosti, potrebne kod proizvodnje, označujemo: postojanost prema vodi, kod pranja, kod kuhanja sa sodom, kod kuhanja pod tlakom, kod bijeljenja s klorom, kod bijeljenja s vodikovim superoksidom, kod merceriziranja, karboniziranja, valjanja, gladčanja, prebojadisavanja i t. d., a kao postojanosti potrebne ili poželjne kod potrošnje: postojanost prema vodi, alkalijama (ulične prašine), trljanju, znojenju, morskoj vodi i t. d.
Na drugim područjima izvan tekstilnog veleobrta, na pr. kod upotrebe u veleobrtu uljenih boja i lakova, dolaze u obzir i postojanosti prema lanenom ulju, prema premazivanju i t. d.
Današnja nastojanja proizvodnje organskih boja iz katrana kamenog ugljena idu za tim, da se na tržište donose proizvodi sa što većim postojanostima, koje su danas često premašile postojanosti najpostojanijih prirodnih boja, a da se proizvodima, koji se od posljednjih desetljeća prošlog stoljeća upotrebljavaju u velikoj mjeri, dadu što točnije karakteristike postojanosti, kako bi ih veleobrt mogao najprikladnije izabrati za upotrebu. M. V-ć.
Bojenje tekstilne robe je postupak, kojim se tekstilna vlakna tako mijenjaju, da reflektiraju samo jedan dio bijelog svijetla i oko onda vidi karakteristične boje. Ova se promjena postizava tako, da se na vlaknu fiksiraju tvari, koje reflektiraju samo jedan dio bijeloga svijetla; to su boje. Samo fiksiranje boja na celuloznom vlaknu je fizikalno-kemijski proces: adsorpcija molekula boje na celulozi, a na animalnom vlaknu kemijski spoj bjelančevine vlakna i molekula boje. Prema vrsti tekstilnog vlakna, t. j. prema tome, da li dolaze u obzir vegetabilna vlakna, koja su sagrađena od celuloze, ili animalna vlakna, koja sačinjava bjelančevina keratin, imamo i različite postupke bojenja, odnosno različite vrste boja. Bojenje se izvodi u vodenim otopinama ili suspenzijama boje tako, da se vlakna ulažu u otopinu i tu gibaju, da boja može jednoliko prijeći iz otopine na vlakno. Proces se može izvoditi i tako, da roba miruje, a tekućina se giba.
Kod bojenja celuloznih vlakna (pamuka, lana, umjetne svile) dolaze u obzir ove skupine boja:
1. Supstantivne boje. One su topive u vodi i imaju direktan afinitet prema celulozi. Boji se u neutralnoj ili slabo alkalnoj kupki uz dodatak kuhinjske ili Glauberove soli i sode, blizu temperature vrenja. Stalnost na vlaknu im je dosta malena, naročito kod pranja; neke od njih su dosta stalne prema svijetlu (Sisius boje).
2. Bazične boje nemaju direktnog afiniteta prema celulozi, pa se njima može bojiti samo posredstvom močila (tanin, katanol). Roba se namače u močilu (tanin, fiksiran sa bljuvaćom sriježi — kalijev stibilotartarat) i nakon toga boji u neutralnoj ili slabo kiseloj kupki uz dodatak octene kiseline. Te se boje odlikuju osobitom živošću i jasnoćom, ali im je stalnost prema pranju i svijetlu, a osobito prema trenju vrlo malena.
3. Boje na močila ili alizarinske boje nemaju također direktnog afiniteta prema celulozi, nego se bojadišu posredstvom močila i to aluminijevih i kalcijevih soli. Moči se uz dodatak sulfuriranih ulja i boji se u suspenziji alizarina. Veoma su stalne prema svijetlu i pranju, ali je skala tonova veoma ograničena.
4. Sumporne boje su netopive u vodi, pa se redukcijom u alkalnoj kupki uz dodatak natrijeva sulfida moraju prevesti u topivu formu. Njima se boji u alkalnoj kupki uz dodatak sode i natrijeva sulfida i soli blizu temperature vrenja. Nakon bojenja se oprana i ižmikana roba podvrgava oksidaciji na zraku, da se topivi leukospoj boje prevede u netopivu boju. Te boje imaju slabu stalnost prema svijetlu, ali su veoma stalne kod pranja.
5. Boje u močama (njem. Küpenfarbstoffe, engl. vat colors, indantrenske boje) su netopive u vodi i također se moraju redukcijom s alkalijama prevesti u vodenu otopinu (moću), t. j. leukospoj boje, koji je obično sasvim druge boje nego osnovna boja, a ima direktan afinitet prema vlaknu. Kod bojenja indantrenskim bojama postoje tri glavna postupka, koji se razlikuju prema količini natrijeve lužine i temperaturi bojenja. To su: IN postupak, sa mnogo NaOH i temperaturom bojenja 50—60ºC; IW sa manje NaOH, boji se kod 40—50ºC; IK ima najmanje lužine, a boji se kod obične temperature 25—30ºC. Poslije bojenja se leukoboja oksidacijom na zraku ili pomoću oksidativnih spojeva (K-bikromat, vodikov peroksid) prevodi u samu boju, koja je netopiva. Ima još specijalnih postupaka, kao na pr. pigmentni postupak, naročito za sintetska vlakna i lan. Tu se roba impregnira veoma fino dispergiranom suspenzijom boje, koja se postizava dodatkom sredstva za dispergiranje (Peregal O,OK). Postepenim dodatkom lužine i hidrosulfita reducira se postepeno boja na samom vlaknu i tu se sasvim jednolično razdijeli i fiksira.
Netopivost je glavni razlog velike stalnosti boja u močama. Kod ovih boja je vrlo važno naknadno obrađivanje u vreloj sapunskoj otopini. Time se postizava pravi ton boje i stalnost. Ove se boje odlikuju velikom stalnošću prema svijetlu i pranju; jedino još neke kombinacije naftolnih boja dostižu jednaku stalnost.
6. Indigosoli. To su esteri leukospojeva indantrenskih boja sa sumpornom kiselinom. Topivi su u vodi i imaju neki afinitet prema celuloznom vlaknu. Njima se boji u neutralnoj kupki, a razvijanje netopive boje provodi se uz dodatak oksidancija (natrijev nitrit) u prisutnosti sumporne kiseline. Sumporna kiselina osapuni ester leukospoja, koji se onda djelovanjem oksidansa prevodi u netopivu boju. Nakon bojenja se vrelim sapunanjem fiksira u močama. Ovamo spada i anilinsko crnilo, koje se odlikuje također velikom stalnošću. Roba se impregnira otopinom anilinklorhidrata uz dodatak oksidirajućih sredstava, te se oksidacija anilina na anilinsko crnilo provede u t. zv. oksidacionim komorama kod temperature 45—50ºC. Tu dolazi do tvorbe zelenog međuprodukta emeraldina, koji se naknadnim provlačenjem kroz rastopinu kalijeva bikromata oksidira na anilinsko crnilo. Naknadnim sapunanjem fiksira se još jače boja na vlaknu.
7. U maloj mjeri upotrebljavaju se još mineralne boje i prirodne boje iz sokova različitog drveća i plodova.
Za animalna vlakna, vunu i svilu upotrebljavaju se ove boje:
1. Kisele boje i supstantivne boje. Bojadiše se kod temperature vrenja u kiseloj kupki i uz dodatak sumporne, octene ili mravlje kiseline te Glauberove soli, kojom se usporava navlačenje boje na vlakno. Stalnost ovih skupina boja je veoma različita; tako su neke stalnije prema svijetlu, druge opet prema valjanju i morskoj vodi. Uglavnom su boje u močama i boje na močila mnogo stalnije od kiselih odnosno supstantivnih boja.
2. Bazične boje upotrebljavaju se rjeđe i to za življe tonove, kad se ne traži osobita stalnost. Njima se boji većinom u neutralnoj kupki kod 80—90ºC.
3. Kisele boje s kompleksno vezanim metalom. Poradi kompleksno vezanog metala (krom i dr.) povećana je stalnost ovih boja, kojima se boji u jako kiseloj kupki kao i s kiselim bojama.
4. Boje na močila (Chromecht, Naphtochrom i alizarinske boje). Tu imamo tri postupka: a) naknadno kromiranje, b) metakrom postupak i c) bojenje na kromiranoj vuni. Konačni produkt kod postupka a) i c) jest stabilan spoj kroma, odnosno drugih metala, kao aluminij, bakar (željezo), i boje. Poradi velike stabilnosti ovog spoja odlikuju se ove boje i velikom stalnošću prema svijetlu, nošenju, trenju, valjanju, pranju, znoju, karboniziranju i dekatiranju.
5. Boje u močama. Ove su boje netopive u vodi, pa se redukcijom uz dodatak natrijeve lužine i hidrosulfita mo raju prevesti u topivo stanje. Boji se u alkalnoj kupki, ali se suvišak alkalija dodaje u formi sode ili amonijaka, jer su animalna vlakna veoma osjetljiva na alkalije.
6. Indigosoli su u vodi topive boje i njima se direktno boji u slabo kiseloj kupki uz dodatak Glauberove soli, Rougalita (formaldehid-sulfoksilat, preparat hidrosulfita), octene ili mravlje kiseline, kod 40—100ºC. Nakon ohlađenja razvija se boja uz dodatak sumporne kiseline i natrijeva nitrita.
7. Naftol AS i analogne boje rjeđe se upotrebljavaju za bojadisanje vune.
Tehnička provedba bojenja. Prema tome, u kojem se obliku nalaze tekstilna vlakna, razlikujemo i različite izvedbe procesa, bojenja. Neispredena vlakna boje se u aparatima, u kojima je roba složena, a otopina boje tiska se kroz nju s pomoću pumpe. Predivo se može bojiti na otvorenim kacama i rukom se provlači kroz boju. Vuneno se predivo boji i u viticama u otvorenim ili zatvorenim aparatima. Namotano predivo na osnovnim valjcima ili križnim kalemima boji se u otvorenim ili zatvorenim aparatima, kroz koje cirkulira boja. Tkanine se boje na jiggerima. Tkanina se provlači kroz tekućinu tako, da se odmotava s jednog valjka, a namotava na drugi i tako provlači izmjenično amo tamo. U aparatima na valjke za ižmikavanje (Foulard, njem. Klotzmaschine) provlači se tkanina kontinuirano kroz koncentriranu otopinu boje i odmah ižmikava između dva ili tri valjka. Kod kaca na čekrk (njem. Haspel-Rufe) provlači se tkanina kroz tekućinu tako, da je čekrk okreće. Aparati za bojenje napravljeni su od najrazličitijih materijala, od drva, željeza, specijalnih čelika i t. d. M. Ž.
Bojenje seljačko. Glavni je predmet seljačkoga bojenja pređa, zatim lončarska roba, uskrsna jaja, manje koža, drvo, tikvica i dr. Bojenje pređe, i to u prvom redu vune, rjeđe lana ili konoplje, vršilo se od davnine po nekim tradicijskim receptima, katkada od samih prirodnih domaćih sredstava, no redovno još i uz pomoć ove ili one kupovne tvari, u prvom redu stipse (slanca, alauna), koja rastopljena u vodi čini pređu prije sama bojenja sposobnom, da boju potpuno primi (katkada se međutim pređa kvasi u stipsi istodobno s bojom). Važnije su biljke za ove domaće boje: za
žutu zanovijet
(Laburnum — stabljika odnosno listovi), srpac
(Serratula tinctoria), žutilovka
(Genista), rjeđe ruj
(Rhus), kora jabuke divljake, šafran i dr., za
crvenu u prvom redu broć
(Rubia tinctorum), zatim ljuske crvenoga luka, od kojih se dobivaju različne osjene crveno-smeđe; za crnu kora johe (jalše), jasena, mladoga hrasta (i šiške hrastove), a uza to zelena galica (vitriol); za
modru boju kupovni indigo (ćivit), rastopljen u vodi, i pređa se u toj boji, toploj, kvasi pa poslije vodom ispire;
zelena se boja dobiva kombiniranim bojenjem modro pa žuto jednim od gornjih načina. Kako su neke t. zv. prirodne boje malo intenzivne, često se ovakvo bojenje tekstilne materije ponavlja po više puta ili se boji dodaju još kakve tvari za pojačanje boje (na pr. lišće breskve sa žutim mesom kod žutoga bojenja; okujina, drozge od kovanja željeza, za crnu boju i dr.). Iza bojenja redovno se tkanina poslije još ispire vodom. Tako bojena pređa, uglavnom domaćim prirodnim sredstvima, zadržava prvobitnu kakvoću i intenzitet redovno dosta dugo (samo neke blijede brže, odnosno mijenjaju se, na pr. od lukovine), dok u novija vremena bojena pređa kupovnim bojama, ponajviše anilinskima, brzo izblijedi, premda je u početku veoma žive, pače nametljivo neukusne, žarke boje. Narodne rukotvorine od bojene pređe iz starijih vremena poznaju se i razlikuju od novodobnih ponajviše upravo po tom intenzitetu boja — one su prve gotovo svagda zagasitije, decentnije. Ribarske mreže na Jadranu narod boji crvenkastomrko s pomoću rastučene borove kore, raskvašene u morskoj vodi. Kožu narodni kožuhari katkada sami boje (inače ponajviše kupuju već obojenu); za smeđu boju služi im johina (jalšina) kora; u zap. Hrvatskoj služile su majstorima za ornamentaciju gumi-boje. Drvo se na selu dosta rijetko boji, katkada zemljanom bojom, inače kupovnom, na pr. crveno fuksinom (često nimalo ukusno kombinirano s rezbarijom) ili žuto šafranom (danas i to napušteno) i slično. Lončarsku robu naši lončari boje dijelom priređenim domaćim bojama: crno s pomoću ječmena ili kukuruzna brašna u vodi raskvašena i sl. (»kaljenje« posuđa), bijelo s pomoću bijele zemlje (zvane i »bajsa«); inače kupovnima, osobito za zelenu, smeđu, žutkastu (druge manje). Pisanice su i danas naročit predmet tradicijskoga seljačkog bojenja (→
batik, → pisanice), i to u prvom redu ovim prirodnim bojama: crveno broćem, crvenkasto do smeđecrveno ljuskama luka (lukovinjem), crno čađom; osim toga upotrebljava se vrlo mnogo za crvenu boju »treščica« ili »varzilo« (brazilsko drvo), koje se mora u vodi raskvasiti, dok se druge boje kupuju gotove u prašcima (a i crvena), u nekim krajevima već odavna, u drugima, konzervativnijim, kao što je na pr. Bosna, tek u novije vrijeme.
LIT.: I. Kršnjavi, Listovi iz Slavonije, Zagreb 1882; Vjesnik Etnografskog muzeja u Zagrebu, III., Zagreb 1937. M. G-i.
Bojenje stakla provodi se na taj način, da se bezbojno staklo pokrije bojenom naslagom, premazivanjem ili umakanjem. Ova se boja ne može skidati ni mehaničkim ni kemijskim putem, a da se ne bi gornji sloj stakla ozlijedio, t. j. sama je boja vezana na staklenoj površini. F. Ko-ć.
Bojenje tijela je elementaran običaj proširen i poznat ne samo kod većine primitivnih, već i kod mnogih kulturnih naroda. Isprva vjerojatno pretežno primjenjivano samo kao ukras ili znak žalosti, dobilo je s vremenom mnogostrano, osobito ritualno i socijalno značenje. Općenito uzevši, bojenje tijela ima kod naroda, osobito onih, koji malo i nikako ne pokrivaju tijelo odjećom, čitav niz zadaća, koje kod Evropljana pripadaju odjeći i nakitu. Glavne funkcije bojenja tijela jesu ove: 1. oznaka žalosti-pokore (Afrika), 2. isticanje ratničkoga izgleda (svuda), 3. oznaka plemena odnosno kaste ili sekte (juž. Azija), 4. zaštita od insekata (Afrika — bijeli pepeo) i zime odnosno vrućine, 5. ukras, osobito kod vjerskih i socijalnih svečanosti, obreda i plesova (osobito razvito na pr. u nekih Australaca). Boje su vegetabilne i mineralne, a najomiljelije su crna i crvena (naročito kod američkih plemena, pa otuda i naziv »crvenokožac«) te nešto žuta i bijela. Sličnu ulogu ima u nekih naroda (na pr. u južnoj Americi) obljepljivanje tijela pahuljicama perja. V. K-k.