AMINI. Ako se u amonijaku zamijene vodikovi atomi alkilskim skupinama, nastaju alifatski amini. Otkrio ih je Wurtz 1848, (iz estera izocijanove kiseline osapunjenjem).

Alifatski su amini bazičkih svojstava i slični su amonijaku. U vodenim otopinama stvaraju alkilamonijev hidroksid i disociraju OH-ione. S kiselinama stvaraju soli. Niži su članovi neugodna mirisa, koji podsjeća na amonijak, viši su gotovo bez mirisa. Neki dolaze u prirodnim organskim spojevima.
Amini nastaju spajanjem amonijaka s alkilhalogenidima »alkiliranje amonijaka« (A. W. Hofmann, 1849):
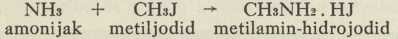
Na taj način dobivamo smjese raznih amina.
Ima više metoda, kako se priređuju čisti amini, na pr. redukcijom alifatskih nitrospojeva (Zinin). Ta je reakcija mnogo važnija za dobivanje aromatskih amina na pr. anilina.
Primarni, sekundarni i tercijarni amini razlikuju se po reakciji sa dušičnastom kiselinom (HNO2).
Alifatski amini. Metilamin, CH3.NH2, dolazi u nekim biljkama, nalazi se u destilatu drva i u produktima razgradnje alkaloida i bjelančevina. Metilamin je plin, miriše po amonijaku, a vri kod —6°. — Etilamin C2H5NH2 vri kod 18°. — Dimetilamin (CH3)2NH i trimetilamin (CH3)3N, nađeni su u salamuri (Heringslake). — Tetrametil amonijev hidroksid, (CH3)4N. OH, vrlo je jaka baza, poput alkalijskih hidroksida.
Aromatski amini nastaju, ako u amonijaku zamijenimo H-atome fenilnim skupinama. Najvažniji je aromatski amin
fenilamin, C
6H
5NH
2, (→
anilin).
— Difenilamin, (C
6H
5)
2NH i
trifenilamin, (C
6H
5)
3N, važni su za proizvodnju organskih sintetskih boja. Od aromatskih diamina poznata su tri izomerna
fenilendiamina C
6H
4(NH
2)
2. Homolozi anilina su
toluidini, C
6H
4(CH
3)NH
2, koji također služe za proizvodnju katranskih boja.