DESTILACIJA (lat. destillatio »kapanje, prekapljivanje«) je pretvaranje tekućine grijanjem u paru i ohlađivanjem ponovno pretvaranje pare u tekućinu. Često se izvodi u kemijskim laboratorijima i u kemijskoj industriji. Uglavnom razlikujemo tri vrste destilacije: običnu ili jednostavnu, frakcioniranu i suhu destilaciju.
Obična destilacija; njome se od teže hlapljivih ili nehlapljivih tvari odjeljuje lakše hlapljiva tekućina, koja se može ispariti, a da se ne raspada.
Smjesa se metne u posudu, ugrije do vrenja, a nastale se pare odvode kroz cijev ili hladilo. Tu se opet zgusnu u tekućinu, koja kapa kao t. zv. destilat u podmetnutu posudu; nju zovemo predloškom.
Destilacija se izvodi ili radi destilata ili radi ostatka, koji je bio otopljen u predestiliranoj tekućini. Tako se na pr. destilira prirodna voda, da se dobije čista voda (Aqua destillata), koja nema više otopljenih anorganskih soli u sebi i koja se mnogo upotrebljava u kemijskim radionicama i u ljekarnama. A kad se na pr. alkoholom ili eterom ekstrahira mast iz kakve tvari, onda se takva tekućina destilira, da bi se odvojila mast, a ujedno opet dobilo čisto otapalo.
Frakcionirana destilacija (prekinuta destilacija); njom se smjesa hlapljivih tekućina različitih vrelišta rastavlja u pojedine sastavne dijelove. Smjesa se metne u posudu za destilaciju s toplomjerom i ugrije do vrenja. Tada izlaze najprije pare one tekućine, koja ima najniže vrelište. Temperatura poraste istom onda, kada je najveći dio te najhlapljivije tekućine već prešao. Poslije toga mora se ukloniti predloška s prvim destilatom i metnuti druga. Sad opet stoji živa u termometru dotle, dok se ne predestilira najveći dio tekućine, koja ima vrelište po redu više od one prve predestilirane tekućine. Kad se počne živa u termometru dizati, opet se mora ukloniti druga predloška i metnuti treća. Tako se radi redom, doklegod se ne odijele svi hlapljivi sastavni dijelovi, koji se onda zovu frakcije. Sve te frakcije obično nisu sasvim čiste, homogene, pa ih treba svaku za se opet frakcionirane destilirati. Ako su vrelišta pojedinih sastavnih dijelova dosta daleko, onda je rastavljanje redovito lakše, a ako su dosta blizu, onda treba smjesu više puta destilirati.
U industriji se primjenjuje frankcionirana destilacija, na pr. za odjeljivanje alkohola od vode, glicerina od vode, za rastavljanje nafte u pojedine frakcije (petrolejski eter, benzin, petrolej za rasvjetu i t. d.).
Frankcioniranom se destilacijom ne može izvesti odjeljivanje takvih tekućina, kojih smjese imaju vrelište više od vrelišta pojedinih sastavnih dijelova. Tako na pr. kod smjese dušične kiseline i vode prelazi kod temperature od 120,5° C stalno smjesa, koja se sastoji od 68% dušične kiseline i 32% vode. Čista dušična kiselina vri kod 87° C, a voda kod 100° C. Slično je i kod drugih kiselina, na pr. kod sumporne, solne, mravlje i t. d.
Suha destilacija; grijanjem se rastavljaju kakve organske tvari bez pristupa uzduha. Kod toga je moguće proizvesti nove produkte, koji mogu biti čvrsti, tekući i plinoviti. Tako se na pr. destilira kameni ugljen i drvo. Kod destilacije kamenog ugljena izlaze metan, vodik, ugljični oksid i t. d., koji se upotrebljavaju za rasvjetu i grijanje; izlazi i katran, koji se opet dalje destilira; zaostaje koks, koji je osobito važan za metalurgiju. Kod suhe destilacije drva zaostaje drveni ugljen, a izlaze dva destilata, katranasti i vodeni. Iz vodenog destilata dobiva se octena kiselina, aceton i metilni alkohol, a iz katranastoga različni kemijski spojevi, među njima mnogi ciklički, kao na pr. benzol, toluol, ksilol, krezol, gvajakol, naftalin, terpeni, politerpeni, smole, fenoli i t. d. U Hrvatskoj se destilacija drva obavlja u tvornicama u Belišću i Tesliću.
Aparati. Najjednostavniji destilacioni aparat sastoji se od retorte, u kojoj se smjesa grije, i od jedne boce kao predloške (v. sl. 1.). Predloška se ohlađuje ili tako, da se polijeva hladnom vodom, ili se metne u posudu, u kojoj je hladna voda. Mjesto retorte uzima se i obična boca, začepljena čepom, kroz koji prolazi koljenasto savinuta cijev, koja vodi u predlošku.
Za destilaciju na malo obično se upotrebljava boca posebnoga oblika, koja ima dugo grlo i na njemu sa strane utaljenu cijev (v. sl. 2.). Takva se boca zove boca za destilaciju. Odozgo se kroz čep provuče termometar. Na cijev sa strane nadoveže se t. zv. Liebigovo hladilo. U široj cijevi hladila nalazi se uža. Kroz užu cijev prolaze pare, a kroz širu, vanjsku cijev, teče obrnutim smjerom hladna voda (princip protustrujanja), koja ohlađuje pare u užoj cijevi. Hladilo se postavi u kosi položaj.
Kod frakcionirane destilacije može se na bocu za destilaciju metnuti još i deflegmator (v. sl. 3.), cijev s više kugala, u kojoj se zgusnu pare manje hlapljivih tvari, tako da kao tekućina teku natrag u bocu, a pare hlapljivije tvari prolaze u cijev i iz nje u hladilo. Tako se tvari brže i potpunije odjeljuju.
Za destilaciju vode u ljekarnama upotrebljavaju se malo veći aparati (v. sl. 4.). Kao destilaciona posuda uzima se kotao, na kojem stoji t. zv. kapak, koji se dalje produžuje u cijev, koja vodi u hladilo. Kao hladilo služi bačva, kroz koju prolazi spiralno savijena cijev ili snop cijevi. Hladna se voda dovodi na dno bačve, a ugrijana voda odvodi se s gornjeg dijela bačve. Slično su građeni i aparati za pečenje rakije.
Različit je materijal, od kojega su načinjene posude za destilaciju. U laboratorijima većinom se upotrebljavaju staklene posude, a u tehnici posude od različita materijala, već prema tvari, koja se destilira. Pazi se na to, da te tvari ne nagrizaju materijal, od kojeg su načinjene posude. Tako se uzima na pr. bakar za destilaciju vode, alkohola, etera, masnih kiselina, ulja i t. d., željezo za katran, benzol, benzin i t. d., aluminij za masne kiseline, ulja i t. d., olovo za razrijeđenu sumpornu kiselinu, emaljirano željezo za hranjiva sredstva.
Posuda za destilaciju može se grijati na različite načine: direktno vatrom, plinovima za grijanje, parom, pregrijanom vodom ili kupeljima od različitih tekućina, od pijeska ili od rastaljenih kovina i električkim putem.
Posude za destilaciju u industriji obično imaju dovodni i odvodni pipac, vodokaz, termometar, manometar, mješalicu i veliki otvor za čišćenje.
Posebni su uređaji za specijalnu vrstu destilacije, t. zv. vakuum-destilaciju, kod koje se uz sniženi tlak destilira u zatvorenim aparatima. Taj se način destilacije primjenjuje, kada se tvari kod viših temperatura rastvaraju, a u »vakuumu« vriju kod niže temperature.
Posebne je vrste destilacija vodenim parama. Ta se destilacija upotrebljava kod mnogih organskih tvari, koje se ne miješaju s vodom, na pr. eterična ulja, ugljikovodici i dr. (v. sl. 5). Kroz tekućinu u posudi za destilaciju vodi se struja vodene pare, pa s parom prelaze i te organske tvari. Često se uzima i pregrijana vodena para, koja se prije ulaza u posudu za destilaciju vodi kroz jako ugrijanu kovinsku cijev.
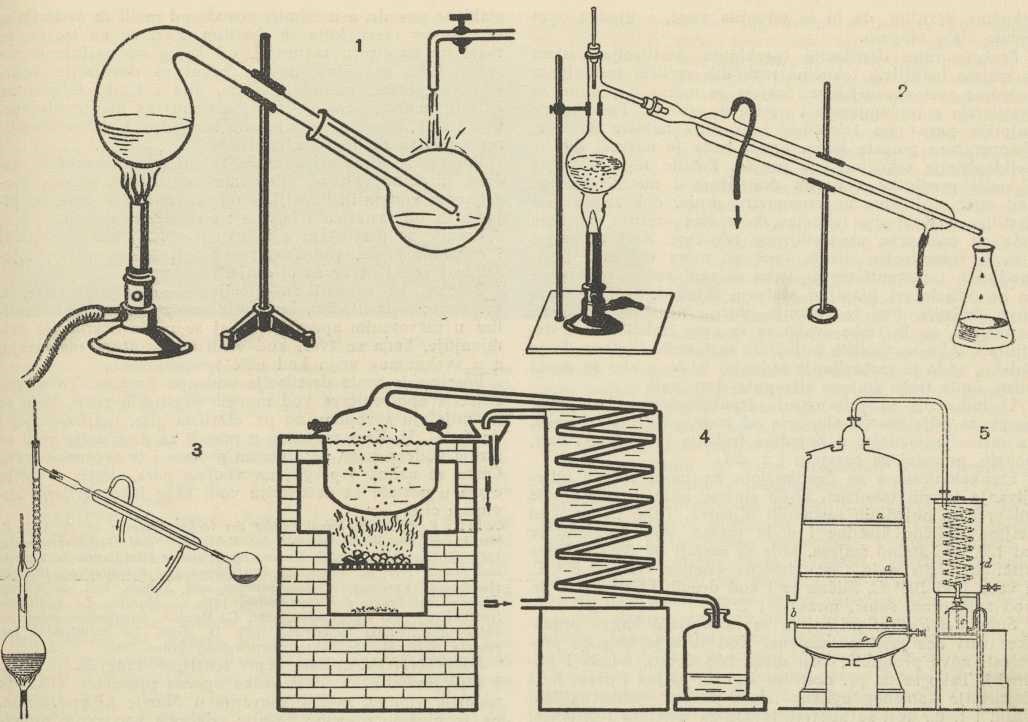 1. Jednostavni aparat za destilaciju. 2. Aparat za destilaciju s Liebigovim hladilom. 3. Aparat za destilaciju s deflegmatorom.
1. Jednostavni aparat za destilaciju. 2. Aparat za destilaciju s Liebigovim hladilom. 3. Aparat za destilaciju s deflegmatorom.
4. Aparat za destilaciju većih količina, osobito vode u ljekarnama. 5. Aparat za destilaciju vodenim parama za eterična ulja.LIT.: F. Ullmann, Enzyklopädie der techn. Chemie, sv. 3., 1916; E. Hausbrand, Die Wirkungsweise der Rektifizier- und Destillierapparate, 1921; C. Rechenberg, Einfache und fraktionierte Destillation in Theorie und Praxis, 1923; K. Thormann, Destillieren und Rektifizieren, 1928; E. Hausbrand, Verdampfen, Kondensieren und Kühlen, 1931; S. Young, Theorie und Praxis der Destillation, 1932; C. Mariller, La destilation fractionnée et la rectification, 1917; C. Mariller, Distillation et rectification des liquides industriels, 1925; D. Ariis, La Distillazione frazionata, 1927; M. Da Ponte, Distillazione, Milan 1930.Z. P-ć.